考题训练(七)__金属资源的利用和保护
|夯 实 基 础|
1.[2017·玉林]下列环境中,铁钉表面最容易产生铁锈的是( )
A.在稀盐酸中 B.在潮湿的空气中
C.在干燥的空气中 D.浸没在植物油中
2.[2017·青岛]下列防锈措施不合理的是( )
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
3.[2017·长沙]下列关于金属材料的说法不正确的是( )
A.常温下,铝能与空气中的氧气反应,在其表面生成致密的氧化铝薄膜
B.铁在干燥的空气中容易生锈
C.硬铝(铝合金)的硬度大于纯铝
D.金属资源的回收利用既保护了环境,又节约了金属资源
4.[2017·河北考试说明样题]工业上将赤铁矿石炼成铁是一个复杂的过程。炼铁高炉中发生的主要反应有( )
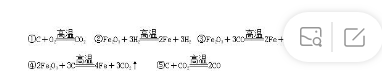
A.②③⑤ B.①③⑤
C.①④⑤ D.②③
5.[2017·北京]用W形玻璃管进行微型实验,如图Z7-1所示。下列说法不正确的是( )
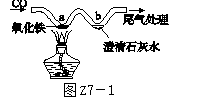
A.a处红棕色粉末变为黑色
B.a处的反应为CO+Fe2O3===2Fe+CO2
C.b处澄清石灰水变浑浊,证明有CO2生成
D.可利用点燃的方法进行尾气处理
6.[2016·永州]工业上用100 t含氧化铁(Fe2O3) 80%的赤铁矿石,理论上可以冶炼出含铁96%的生铁的质量是( )
A.56 t B.58.3 t C.70 t D.72.9 t
7.[2017·唐山滦南区一模]铁制品在我们家庭中应用广泛,现有从洗澡间拆下的两根生锈的铁管:A管里面生了很多锈,B管外面生锈严重,请你根据所学知识回答问题。
(1)铁生锈的条件是________________________,铁锈的主要成分是____________(写化学式)。
(2)你判断一下A、B两管哪一个原来是供热水的管道:________,你判断的理由是____________________________________。
(3)通常用稀盐酸来除铁锈其反应方程式为__________________________________。
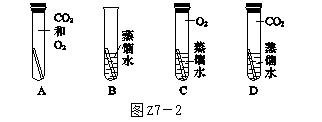
8.[2017·河北考试说明样题]铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3]。根据铜锈的主要成分中含有氢元素和碳元素,可以判断出铜生锈需要空气中的________(填化学式)。若要探究"铜生锈是否需要空气中的氧气",在图示实验中,只需完成________(填序号)两个实验即可达到目的。
|能 力 提 升|
1.[2017·成都节选]工业上炼铁、炼钢和轧制钢材的主要流程如图Z7-3所示。
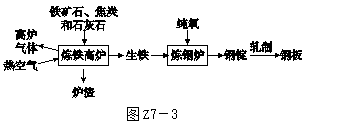
已知生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(1)发生的反应①3CO+Fe2O3eq \o(=====,\s\up7(高温))2Fe+3CO2、②Fe2O3+3Ceq \o(=====,\s\up7(高温))2Fe+3CO中,属于置换反应的是________(填序号,下同),用于高炉炼铁的原理是________。
(2)炼铁的固体原料需经过粉碎,其目的是__________________________________。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是______________。
(4)炼钢炉中,通入纯氧的目的是__________________________________。
2. [2017·安徽]某研究小组为探究"影响铁制品锈蚀快慢的因素",取同浓度的稀氨水和稀醋酸用如图Z7-4装置完成表中实验,回答下列问题。
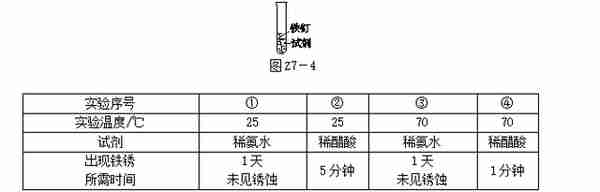
(1)铁锈的主要成分是__________(填化学式)。
(2)实验②和④可探究__________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是____________(填实验序号)。
(3)根据表中实验现象得出的结论是_____________________________________________(写出1点即可)。
(4)影响铁制品的锈蚀快慢除上述因素外,还有________(写出1点即可),请设计实验方案___________________________________________。
3.[2016·绥化]某同学用如图Z7-5所示装置,进行有关碳及其氧化物的实验(图中夹持装置已略去),在完成气密性检査后加入药品,并已在装置中充满二氧化碳。

填写表格中的空白内容:
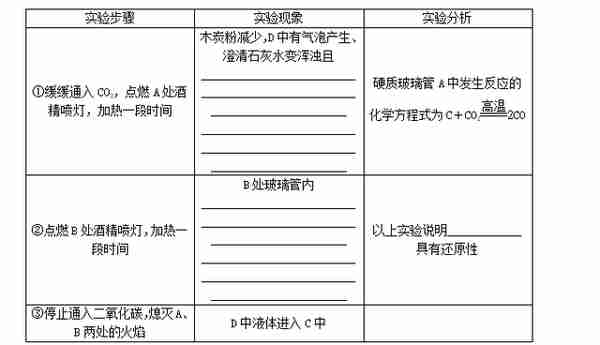
(2)有同学认为该装置需要添加尾气处理装置,你认为是否需要并说明理由:_____________________________________________________________。
4.[2017·天津节选]金属材料广泛应用于生产生活中。
(1)A~G是初中化学常见的物质。已知A为黑色固体单质,B为红棕色粉末,C为无色气体,G为紫红色固体单质,它们的转化关系如图Z7-6所示,回答问题。
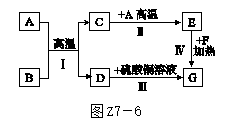
①写出化学式:A________;B________。
②反应Ⅱ的化学方程式为________________________________________________________________________。
③反应Ⅲ的化学方程式为________________________________________________________________________。
(2)用1600 t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量为多少?(结果保留至小数点后一位)
参考答案
|夯实基础|
1.B [解析] 铁钉生锈是铁与空气中氧气和水共同作用的结果,故在潮湿的空气中铁钉最容易生锈,铁锈蚀最快。
2.B [解析] 铁生锈需要氧气和水,钢管存放在干燥的地方,由于缺乏水,钢管不易生锈;盐水能加速铁的锈蚀;铁锈疏松多孔,易吸附空气中的氧气和水,加速铁的锈蚀,因此,及时清除铁制品表面的锈渍,可以减缓铁的锈蚀;在铁制品表面镀上一层不易锈蚀的金属,使铁与空气中的水和氧气隔绝,能防止铁生锈。
3.B [解析] 铁生锈需要与氧气和水同时接触,干燥的空气中缺少水,因此,铁在干燥的空气中不易生锈。
4.B
5.B [解析] B项中化学方程式缺少反应条件,且化学方程式未配平。
6.B
7.(1)与氧气和水接触 Fe2O3
(2)B 热水管中水含氧量少,内部不容易生锈,而外面温度高,铁生锈严重
(3)Fe2O3+6HCl===2FeCl3+3H2O
8.H2O和CO2 BD
|能力提升|
1.(1)② ①
(2)增大接触面积,加快反应速率
(3)N2
(4)和碳反应,降低生铁中的含碳量
2.(1)Fe2O3
(2)温度 ①②(或③④)
(3)相同酸性条件下,温度越高,铁制品锈蚀速率越快(或碱性条件下,铁制品不易锈蚀)
(4)氧气浓度(合理即可)
在相同温度下,在上述试管中分别充入空气和氧气并塞上橡胶塞,观察出现铁锈所需的时间
[解析] (2)实验②和④除温度不同外,其余条件均相同,故这2个实验对比可得出温度高低对铁制品锈蚀快慢的影响;若想探究试剂酸碱性对铁制品锈蚀快慢的影响,则需在不同酸碱性环境下对比铁制品生锈速率的快慢,可对比实验①②或③④来得出结论。(3)由表中数据可知,在碱性环境下(实验①③),铁制品不易生锈;在酸性环境下(实验②④),温度越高,铁制品生锈速率越快。(4)影响铁制品锈蚀快慢的因素除上述试剂的酸碱性、温度高低外,还有盐溶液存在与否、氧气浓度大小等因素。若要探究氧气浓度对铁制品锈蚀快慢的影响,可向题给装置中分别充入空气和氧气并塞上橡胶塞,观察出现铁锈所需的时间即可。
3.(1)澄清石灰水沿右侧导管进入E
红色粉末变为黑色 碳、一氧化碳
(2)不需要,未反应的CO进入D装置,不会逸散到空气中
[解析] (2)本题中的化学反应是二氧化碳与碳在高温条件下生成一氧化碳,一氧化碳高温还原氧化铁,D中二氧化碳使澄清石灰水变浑浊,同时收集未反应的一氧化碳气体,所以不需要添加尾气处理装置。
4.(1)①C Fe2O3 ②CO2+Ceq \o(=====,\s\up7(高温))2CO
③Fe+CuSO4===FeSO4+Cu
(2)解:设理论上可炼出含铁96%的生铁的质量为x。
3CO+Fe2O3 eq \o(=====,\s\up7(高温)) 2Fe+3CO2
160 112
1600 t×80% x×96%
eq \f(160,112)=eq \f(1600 t×80%,x×96%) x=933.3 t
答:理论上可炼出含铁96%的生铁的质量为933.3 t。
[解析] (1)由A为黑色固体单质,B为红棕色粉末,C为无色气体,可推断反应Ⅰ是碳还原氧化铁的反应,则A是碳,B是Fe2O3,C是CO2,D是Fe;二氧化碳和碳在高温条件下反应生成一氧化碳,则E是CO;反应Ⅲ是Fe+CuSO4===FeSO4+Cu,则G是Cu,反应Ⅳ是CO还原氧化铜,则F是CuO。
